「救命的」腫瘤基因檢測:離爆發(fā)還有多遠?
“技術還需要更成熟。”
二代基因測序技術(NGS)很大程度滿足了臨床需求,因此它從原先的實驗室科研、藥企服務走向了臨床應用。不過這對NGS企業(yè)提出了技術和商業(yè)化賽道選擇上的更高的要求。
NGS臨床應用始于無創(chuàng)產(chǎn)前檢測(NIPT),NIPT相關業(yè)務在華大基因(行情300676,診股)(300676.SZ)、貝瑞基因(行情000710,診股)(000710.SZ)營收中占很大比例。NIPT技術階段性成熟,并且檢測后有干預手段(人為終止妊娠等)可形成閉環(huán),其滲透率還將逐步提高。
遺傳病、生殖健康領域有巨大需求,胚胎植入前遺傳學基因檢測(PGT)實現(xiàn)了技術進步,NGS已被用于輔助生殖的優(yōu)孕優(yōu)生領域。但由于檢測企業(yè)的技術門檻高、樣本數(shù)據(jù)正在積累階段,這類初創(chuàng)公司占比較少。
「剛需」吸引融資
在NGS較分散的應用市場中,腫瘤精準診斷在公開投資數(shù)量、金額上,是近年最熱的投資領域,而獲得融資的公司,業(yè)務多圍繞腫瘤早篩、腫瘤伴隨診斷用藥而展開。無論是患者還是醫(yī)生都將因此受益。
首先,分子級的早期診斷可以改善癌癥預后,極大提升治療成功率、降低成本、避免病情復雜化。以腸癌早篩來看,即使經(jīng)過手術、放化療、靶向治療等綜合治療,患者的5年生存率低于40%;但早期結直腸癌治療后,5年生存率可超過90%。病人花費上看,晚期的結直腸癌治療除了手術以外還要進行化療,加上所用藥物,總費用約超過30萬元。而早篩的診斷試劑盒價格在未來幾年最低可達到幾百元。并且診斷試劑盒的使用過程無痛無創(chuàng)。目前常規(guī)的體檢手段只能針對蛋白抗體檢測以進行初篩,無法達到對很多腫瘤病癥的“早篩”。
再以肝癌早篩為例,中國大量的乙肝患者中,有一部分會轉化為肝癌。如果在病情惡化前盡早篩查隱患,采取手術等干預手段,對患者健康和國家醫(yī)保都將意義重大。我們也向業(yè)內(nèi)人士了解到,目前肝癌早篩試劑盒靈敏度和特異性較好,肝癌或肝炎治療的醫(yī)療機構接受度較高,所以大量的臨床醫(yī)生也會參與到早篩試劑盒的使用,這對早篩產(chǎn)品應用在其他適應癥的檢測也起到積極作用。
其次,在腫瘤治療的不同階段,基于基因檢測的伴隨診斷(CompanionDiagnostics,CDx)可幫助醫(yī)生評價患者是否適合某種藥物的檢測,因為腫瘤用藥需要判斷藥物與患者的匹配度來向精準發(fā)展。
伴隨診斷的方法中,目前在中、美最廣泛使用的是PCR法,其細分技術平臺主要用于基因層面突變、缺失、插入等的檢測。PCR法主導的伴隨診斷市場格局已較為明確。而NGS 癌癥伴隨診斷可以在一次單一檢測中同時檢測到與患者癌癥相關的所有基因組改變和生物標志物,較傳統(tǒng)癌癥診斷手段來說,顯著降低了成本,又提高了準確性。
腫瘤精準檢測國內(nèi)規(guī)模化起步
相關的技術與商業(yè)化始于美國市場。Exact Sciences(EXAS.O)曾推出全球第一款腫瘤早篩產(chǎn)品Cologuard ——一種非侵入性、基于糞便 DNA 的大腸癌篩檢產(chǎn)品。Exact Sciences是專注于非入侵性大腸癌篩檢的分子診斷公司,于2001年在納斯達克上市。
美國Guardant Health(GH.O)專注于液體活檢,業(yè)務包含晚期癌癥檢測、高風險人群早期癌癥篩檢、復發(fā)患者檢測。其主要的創(chuàng)收產(chǎn)品GUARDANT 360針對晚期癌癥檢測,輔助醫(yī)生選擇最佳靶向治療方案。其他三個未商業(yè)化產(chǎn)品僅用于實驗室研究及制藥公司新藥開發(fā)。公司于2018年在納斯達克上市。
另一家腫瘤伴隨診斷公司FoundationMedicine(退市后被羅氏收購)曾推出全球首個獲批上市的基于NGS的伴隨診斷產(chǎn)品FoundationOne CDx,它可用于泛癌癥臨床伴隨診斷,是首款NGS體外診斷產(chǎn)品,能對任何實體腫瘤進行診斷。公司目前的三個產(chǎn)品均針對腫瘤伴隨診斷和液體活檢。
基因測序系統(tǒng)供應商巨頭Illumina(ILMN.O)與Memorial Sloan Kettering癌癥中心合作組建血液基因檢測公司Grail,研究方向為基于液體活檢(血液)泛癌種檢測、乳腺癌、肺癌等早篩,2019年公司開始了商業(yè)化籌備。
再看國內(nèi)市場,今年,兩家中國腫瘤NGS基因檢測公司燃石醫(yī)學(BNR.O)和泛生子(GTH.O)在美國上市。更多同賽道公司即將上市,亦或是近年獲億元人民幣級大額融資。世和基因已于今年4月提交上市申請,近期將完成科創(chuàng)板上市。思路迪診斷已于上半年完成Pre-IPO輪融資。
臻和科技于去年10月完成D輪融資。諾輝健康在2019年5月完成6600萬美元C輪融資,今年4月已完成D輪,也正在籌備上市。以遺傳疾病基因診斷為主業(yè)的華大基因、貝瑞基因也全面布局了腫瘤早篩、腫瘤伴隨診斷相關業(yè)務。
針對各類癌種的相關標志物和靶向以及免疫治療的種類已經(jīng)比較豐富,因此NGS腫瘤伴隨診斷可應用于更多的癌種。
國內(nèi)外研發(fā)有突破后,NGS腫瘤診斷加快融資步伐。業(yè)內(nèi)的公司基本都在同一起跑線上,不過商業(yè)化路徑有所不同。
燃石醫(yī)學是目前中國排名第一的NGS腫瘤伴隨診斷提供商,2019 年收入3.8 億元,在中國NGS基因分型市場中的肺癌細分領域市場份額為31%,公司今年啟動了泛癌種早檢研究工程。泛生子覆蓋從早期篩查、到診斷治療建議、再到持續(xù)監(jiān)測和持續(xù)治療的全過程癌癥護理,未來研發(fā)方向包括肺癌、肝癌、消化道癌癥的早篩。由于研發(fā)開支高,兩家公司未盈利。
世和基因是最早實現(xiàn)盈利的腫瘤基因檢測公司,除了腫瘤伴隨診斷以外,其收入來源還包括抗感染檢測業(yè)務。思路迪診斷在腫瘤的早期診斷、伴隨診斷領域到動態(tài)監(jiān)測都開始布局,其中伴隨診斷業(yè)務創(chuàng)收過億,其早期診斷產(chǎn)品預計明年上市后,將創(chuàng)造新的銷售額。諾輝健康讓用戶在居家場景下完成癌癥的早期篩查,切入的是腸癌、肺癌、宮頸癌等細分賽道,發(fā)布的主要產(chǎn)品則包括常衛(wèi)清、噗噗管、費證清、常衛(wèi)友、宮證清等,其預測的盈利時間在2020年年末或2021年年初。
腫瘤早篩技術的已知與未知
浩悅資本合伙人李逸石表示,從體量規(guī)模、增速上看,腫瘤早篩還處在初步的發(fā)展階段,仍會有一批顛覆性的公司出現(xiàn),也會伴隨著淘汰。不過大腸癌早篩已然領跑:康立明生物的大腸癌早篩輔診試劑盒(熒光PCR法)經(jīng)國家藥監(jiān)局批準上市;銳翌生物也在報證階段,有望成為國內(nèi)第二家腸癌早篩IVD獲批企業(yè)。
在Exact Sciences的Cologuard于2014年獲批上市的背后,其研發(fā)落地的關鍵人物之一則是康立明生物的創(chuàng)始人鄒鴻志。鄒鴻志曾在美國梅奧醫(yī)學中心從事博士后研究工作,在Exact Sciences擔任研發(fā)總監(jiān)時,他主導了CologuardTM糞便腸癌篩查試劑盒的開發(fā)。康立明生物的腸癌檢測試劑盒“長安心”不僅對標Cologuard,其特異檢測性97.85%還高于Cologuard(86.6%)。
當然,其他大癌種的早篩技術需要企業(yè)扎實投入研發(fā)。傳統(tǒng)的腫瘤檢測手段涵蓋血清腫瘤標記物、醫(yī)學影像學檢查、組織活檢,其對早期腫瘤的篩查準確度有很大局限,組織活檢則需侵入患者體內(nèi)取出病變組織進行診斷。
相比下,液體活檢是突破性的檢測技術,在早期癌癥篩查、分子靶向藥用藥指導檢測、腫瘤復發(fā)檢測上都能提供比傳統(tǒng)手段更有效的臨床指導。醫(yī)生可以在影像學技術還未能發(fā)現(xiàn)病灶時就在外周血中檢測到腫瘤細胞或腫瘤相關的遺傳物質(zhì),再根據(jù)最新測序技術探明導致癌癥的突變,從而可“預知”癌癥。
而作為體外診斷一個分支,液體活檢通過血液或尿液等對癌癥等疾病做診斷,優(yōu)勢在于通過非侵入性取樣方式降低了對人體的傷害。但開發(fā)基于液體活檢的早期癌癥檢測測試非常困難,其具有測試在臨床上有用所需的靈敏度和特異性。強臨床需求下,液體活檢自然是NGS潛力最大的應用市場之一,也是中美企業(yè)研發(fā)的方向。
檢測可及性增加,但業(yè)務難免同質(zhì)化
很多企業(yè)投身于NGS腫瘤伴隨診斷,但NGS腫瘤伴隨診斷在中國的滲透率仍然很低,主要是由于醫(yī)生的意識不高和靶向治療的可用性有限。在 2019 年,中國僅有6.4%的晚期癌癥患者和被建議進行癌癥基因分型檢測的癌癥患者采用 NGS 癌癥伴隨診斷檢測,而在美國這一比例達到 23.5%。
另外,有參與醫(yī)藥投研的資深人士也表示,腫瘤伴隨診斷領域,目前能立足于市場的公司已經(jīng)證明其技術和業(yè)務優(yōu)勢,不過目前各公司的技術差異不大,不同之處主要存在于基因檢測服務商主動選擇的渠道、科室的差別。
這也意味著,伴隨診斷方面,檢測企業(yè)在銷售側將會投入更多。
隨著伴隨診斷規(guī)模擴大,這里不得不提到基因檢測企業(yè)開展腫瘤伴隨診斷(及早篩)的模式:中心實驗室LDT(院外市場)和院內(nèi)實驗室(院內(nèi)市場)模式。
據(jù)興業(yè)證券(行情601377,診股)總結,若樣本及費用不經(jīng)過醫(yī)院直接交給第三方實驗室,則按照業(yè)內(nèi)習慣稱為院外市場。院外市場的醫(yī)學實驗(Laboratory Developed Test, LDT)需經(jīng)衛(wèi)生行政部門批準,但所用試劑可無需國家藥監(jiān)局批準,在監(jiān)管層面上準入門檻低;可診斷罕見靶點或基因,滿足科研及學術需求。LDT僅限所在醫(yī)學檢驗部門內(nèi)部使用,不得作為檢測試劑出售給任何其它醫(yī)學檢驗部門、醫(yī)院及個人。LDT因由實驗室自行研發(fā),各機構間同一項目檢測性能和結果往往存在差異。
中心實驗室是燃石醫(yī)學收入的核心業(yè)務,與燃石醫(yī)學合作的醫(yī)院收診的癌癥患者的醫(yī)生在診治過程中使用燃石醫(yī)學的NGS中心實驗室服務——將患者的液體活檢或組織樣本運送到燃石醫(yī)學的實驗室進行檢測,然后根據(jù)檢測結果設計治療計劃。公開資料顯示,2019年燃石醫(yī)學在院外市場的份額為80%左右。
若樣本及費用由患者流向醫(yī)院,則稱為院內(nèi)市場。院內(nèi)市場是合規(guī)市場,醫(yī)院采購試劑均需通過國家藥監(jiān)局批準(即采購“有證產(chǎn)品”IVD),價格相對合理,渠道黏性高。腫瘤基因檢測產(chǎn)品按照國家三類醫(yī)療器械管理,有最嚴格的注冊審批程序,從臨床評估到批準上市至少需3年以上時間。
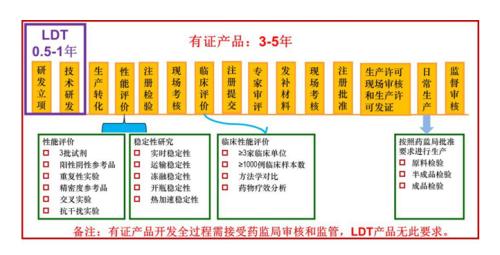
有證產(chǎn)品LVD與LDT服務對比(來源:醫(yī)學檢驗網(wǎng))
由此,從診斷風險上說,對于已有獲批試劑的檢驗,院方會優(yōu)先使用IVD有證產(chǎn)品,但仍有很多臨床需求尚未滿足的檢驗則可有條件使用LDT實驗室自建項目。
目前,在伴隨診斷用藥方面,有燃石醫(yī)學、諾禾致源、世和基因以及艾德生物(行情300685,診股)(300685.SZ)四家診斷公司開發(fā)的腫瘤NGS檢測試劑盒獲批。而在腫瘤早篩的IVD產(chǎn)品里,使用糞便DNA檢測的康立明生物,其大腸癌早篩檢測試劑盒獲批上市。血檢腫瘤早篩IVD產(chǎn)品在國內(nèi)還處于空白。
約印醫(yī)療基金創(chuàng)始合伙人、CEO鄭玉芬表示,在NGS方面,政策從保守轉向慢慢放開,國家對實驗室做了規(guī)范化管理,實施牌照,對技術予以合規(guī)。隨著大家技術的成熟,國家對試劑盒的審批也會加大推進,醫(yī)院拿到試劑盒就可以在醫(yī)院里進行檢測,不用把樣本送到實驗室,這會大大推進整個檢測的范圍和檢測的可及性。
在腫瘤伴隨診斷IVD產(chǎn)品的代表之一是泛生子。泛生子LDT和IVD同時推進。泛生子的IVD 服務在2019 年實現(xiàn)收入3500萬元,其檢測方法和平臺數(shù)量在中國NGS的癌癥診斷和檢測行業(yè)中排名第一,因此它在癌癥分子診斷市場較為領先。上文提到的肺癌、肝癌等腫瘤早篩方向,泛生子也計劃先以IVD形式注冊,形成市場轉化。
附注:文中提到的熒光PCR法(熒光定量PCR技術,qPCR)是分子診斷的方法之一,比NGS應用更早地應用。qPCR只能夠通過標準曲線和標準品進行相對定量,無法做到精準絕對定量。NGS可以一次對幾十萬到幾百萬條DNA分子進行序列測定。
